-
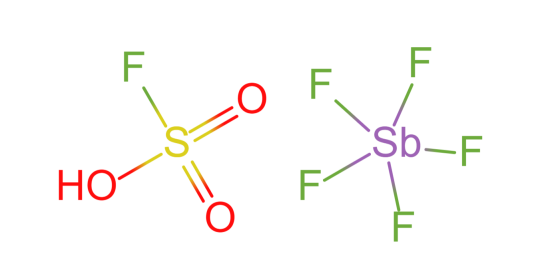
氟锑磺酸 编辑
氟锑磺酸,又称魔酸,是一种超强酸,是一种路易斯酸五氟化锑和一种质子酸氟磺酸的混合物,化学式为SbF5·HSO3F,为无色透明的粘稠液体,含杂质时为淡黄色、棕色甚至是黑绿色。有明显的刺激性气味,纯净的氟锑磺酸密度大致为3.61-3.82 g/mL,无固定熔沸点。当质子酸路易斯酸混合时,其酸的强度增大。魔酸(SbF5·HSO3F),是由两种或两种以上的含氟化合物组成的溶液。比如氟硫酸和五氟化锑按1:0.3(摩尔比)混合时,它的酸性是无水硫酸的1亿倍;按1:1混合时,它的酸性是无水硫酸的1019倍。能溶解不溶于王水的高级烷烃蜡烛。酸碱中和反应的实质是质子的传递反应。超酸是指酸性比普通无机酸强106~1010倍的酸。魔酸(HSO3F-SbF5)是已知除氟锑酸(HF-SbF5)外最强的超酸,许多物质(如H2SO4)在魔酸中可获得质子(即质子化)。SbF5和HF以0.2:1的摩尔比混合时酸度以达到100%硫酸的109倍以上,随着SbF5的比例增加酸度还能增强。魔酸,应当用聚四氟乙烯制的容器盛放,一般讲超强酸是指比100%的硫酸酸性更强的酸。
物理性质
电导率(S/m,25ºC):1.2×10-8
密度:3.61-3.62g/cm3
化学性质
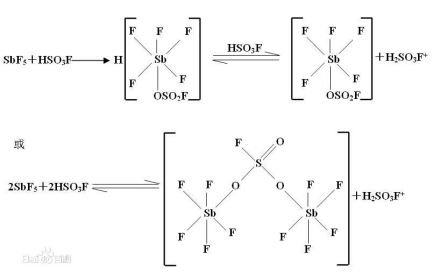 魔酸
魔酸
氟锑磺酸酸性极强,以至于高氯酸在其中都会被质子化:
HClO4+ HSbF5(OSO2F)= -+ +
在这种酸性环境下,一般情况下很多无法进行的有机化合反应可以顺利进行。故氟锑磺酸常作为现代化工合成反应的催化剂。
超强酸能向链烷烃供给质子,使其质子化形成碳正离子。
超强酸对链状卤素和硫阳离子的研究提供了一个优良的溶剂介质。
氟锑磺酸还是一种良好的溶剂和腐蚀剂,可以将包括金、铂在内的极不活泼金属氧化溶解。氟锑磺酸通常储存在聚四氟乙烯的容器内。在室温下氟锑磺酸和玻璃作用剧烈,并能溶解烃类有机物,可以将有机含氧化合物脱水炭化,但和含铅塑料玻璃(一种状似玻璃的透明有机含铅有机材料,主要成分是全氟聚苯乙烯、聚四氟乙烯、和二氟化铅)反应很慢,故一般用含铅塑料玻璃制成的细口瓶盛装。
氟锑磺酸酸使某些很难质子化的物质(如高氯酸)质子化,进一步制备含有-ClO3基团的有机物:
HClO4 + H+= +
++H+=++ +
C6H6+ += +
+ - H+ =C6H5ClO3
氟锑磺酸酸使高级烷烃质子化,催化烷烃裂解:
(CH3)3CH + H → (CH3)3C + H2;
(CH3)4C + H → (CH3)3C + CH4
氟锑磺酸酸含有羟基的有机物(如醇、酚、羧酸等)质子化,进一步脱羟基化。
R-OH + 2H = R+(碳正离子) + +
强氧化剂:Sb(V)氟化物例如SbF5具有一定的氧化性,加上它超强的酸性,大大增加了氧化能力,能够氧化腐蚀多种金属。要注意的是,氟锑磺酸是无水体系,当氟锑磺酸与大量水混合时发生强烈反应,失去超酸性。
性质与稳定性:当质子酸与路易氏酸混合时,其酸的强度增大。典型的代表是氟硫酸与五氟化锑两者以1:1的混合体系,被称为魔酸。在室温下为无色透明的黏稠状液体,它是一种最强的酸。在魔酸中几乎所有的有机化合物都可以发生离子化。魔酸组成之一的SbF5为无色黏稠状液体,与湿气接触产生白烟,是一种非常强的路易氏酸,能与多种化合物形成加成产物。
超强酸在化学和化学工业上,有应用价值,它既是无机及有机的质子化试剂,又是活性极高的催化剂。而由于超强酸的酸性和腐蚀性强得出奇,所以过去一些极难或根本无法实现的化学反应,在超强酸的条件下便能顺利进行。比如正丁烷,在超强酸的作用下,可以发生碳氢键的断裂,生成氢气,也可以发生碳碳键的断裂,生成甲烷,还可以发生异构化生成异丁烷,这些都是普通酸做不到的。
可以预料,随着这些具有超常酸性和腐蚀性超强酸的相继问世,化学和化学工业将会迅速走进新时代。
氢键供体数量:1
氢键受体数量:9
可旋转化学键数量:0
互变异构体数量:0
拓扑分子极性表面积:62.8
重原子数量:11
表面电荷:0
复杂度:130
同位素原子数量:0
确定原子立构中心数量:0
不确定原子立构中心数量:0
确定化学键立构中心数量:0
不确定化学键立构中心数量:0
共价键单元数量:2
氟锑酸(1:1)(1990)(H0=−28)
魔酸(五氟化锑合氟磺酸(1:1),简称氟锑磺酸)(1974)H0=-26.5)
碳硼烷酸(1969)(H0=−18.0)
氟磺酸(1944)(H0=−15.1)
三氟甲磺酸(1940)(H0=−14.6)
浓高氯酸(H0= -13.0)
魔酸(五氟化锑合氟代磺酸,简称氟锑磺酸)的酸性是除氟锑酸外最强的,值得注意的是魔酸是混合物,由HSO3F与SbF5的混合配置而成的,另外含氧酸的确切定义是由O、H与一中心原子组成的可自主电离出质子的物质,其酸性最强的配置比为HSO3F:SbF5=2:98(摩尔比)。
其酸性强的机理:首先HSO3F(氟磺酸,或单氟硫酸)的酸性本身比HClO4强,不过在水溶液中由于拉平效应它们的水溶液酸性强度是一样的(就像浓度一样的硝酸溶液和盐酸溶液酸性一样,我们一般认为HNO3与HCl的酸性是不可区分的,但事实上不是),在HSO3F电离出H+后由于O、F强拉电子作用(诱导效应)使负电荷电荷较均匀的分布于整个离子,减弱了质子对阴离子团的库仑力使质子能更好的电离出去。
然后是SbF5的作用,SO3F-中由于存在S→O的配位键,使O上带较明显的负电,SbF5中由于F对Sb的诱导效应,使Sb带较强的正电性,且Sb上存在一个5p空轨道(为强Lewis酸)正好可以与SO3F-中的O上的孤电子对形成较强的配位键。就是说存在S→O→Sb,这样负电荷就扩散到了更大区域,并且受到了SbF5基团对负电荷的很好屏蔽,最多SO3F-可以与3个SbF5配合。但是配合度越低越稳定,这是因为SbF5基团太大互相抵触,使得SO3F-不能更好与太多的SbF5很好配合,因此可以解释魔酸中SbF5的量相当大,这样H+对该配合物基本不存在库仑力了,所以使得H+变得相当自由,甚至可以“趴在”电子云密度相对较大的C—H键上形成二电子三中心键很不稳定易分解生成碳正离子与H2。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。