-
共用电子对 编辑
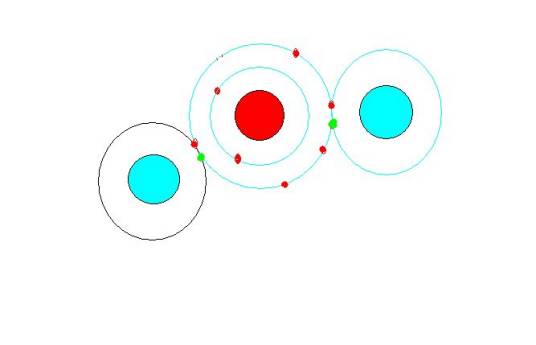
在化学反应中元素的原子都有使最外层电子达到稳定结构的趋势。在共价键理论中,成键的两个原子的轨道发生重叠,一对电子位于两个原子之间。例如氯元素的原子在化学反应中易得到一个电子,而氢元素的原子容易失去一个电子形成稳定结构、这两种元素的原子相互作用的结果是双方各以最外层一个电子组成一个电子对,为两原子共用,在两个原子核外的空间运动,从而使双方都达到稳定结构。这种电子对叫做共用电子对。
因原子核对电子吸引力的强弱而使电子对有所偏移,电子对偏向一方略显负电性,偏离一方略显正电,相互吸引形成共价化合物,但作为分子整体仍是电中性。
中文名:共用电子对
外文名:bonding pair
概述:使最外层电子达到稳定结构的趋势
相关问题:电子对就在当中不偏移称非极性键
形成原因:电荷的分布不均
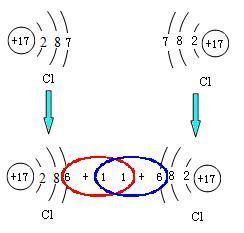 共用电子对
共用电子对
原子在最外层是8电子时是稳定结构(氢、氦除外),所以原子会尽量从外界获得电子以形成八电子稳定结构。金属的失电子能力比较强,非金属的得电子能力比较强。所以他们结合就会直接得失电子形成离子。而得失电子能力差不多的元素相遇,它们不能直接进行电子的得失,所以就会各拿出一个或多个电子形成共用电子对。这时候,每一个电子都同时属于两个原子,它在两个原子核外的空间运动,同时绕两个原子核运转,使原子的最外层有八个电子。而因原子核对电子吸引力的强弱而使电子对有所偏移。电子对偏向一方略显负电性,偏离一方略显正电。这就是共用电子对。
1、本站所有文本、信息、视频文件等,仅代表本站观点或作者本人观点,请网友谨慎参考使用。
2、本站信息均为作者提供和网友推荐收集整理而来,仅供学习和研究使用。
3、对任何由于使用本站内容而引起的诉讼、纠纷,本站不承担任何责任。
4、如有侵犯你版权的,请来信(邮箱:baike52199@gmail.com)指出,核实后,本站将立即删除。